初中与yu小学相比,科目更多了,需要学xue习的内容也更多了,学习压力更大。各科都有知识量liang大、系统性强、综合性强以及能力要求qiu高等特点,知识点是零乱的,不利于yu记忆和掌握。
然而,学霸们能学习xi好,自然有自己的方fang法。一位女学霸就用“红线”把ba知识“串”起来,这样,各科知识结jie构就一目了然了le。
今天,把这位女学霸的知识总结分享给大家jia,方便同学们整体把握wo知识之间的联系。如果guo都掌握了,你的学习成绩一定会更geng上一层楼!!

语文
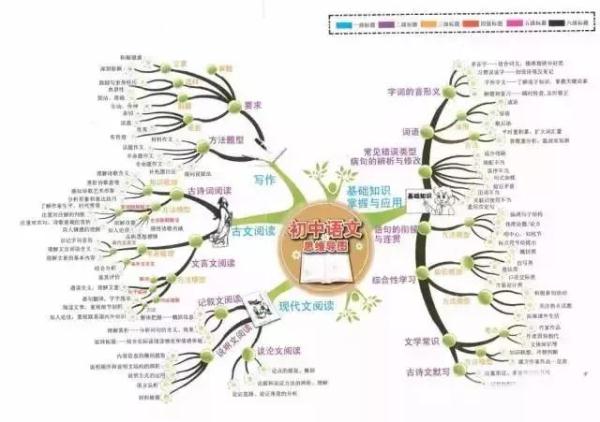
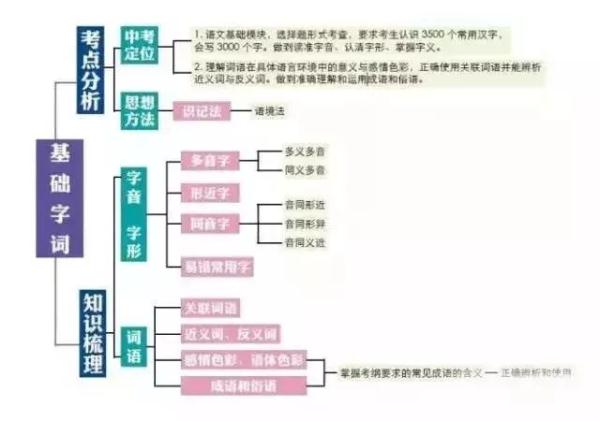
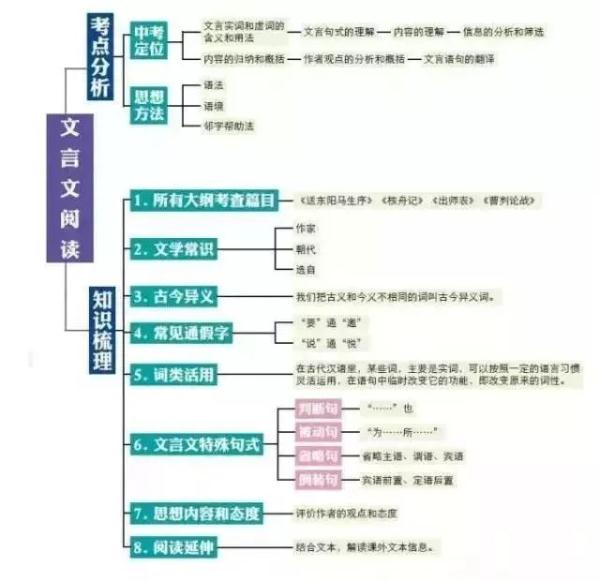

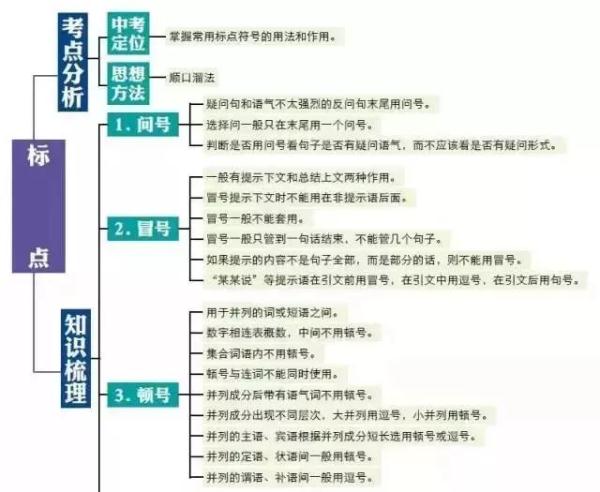
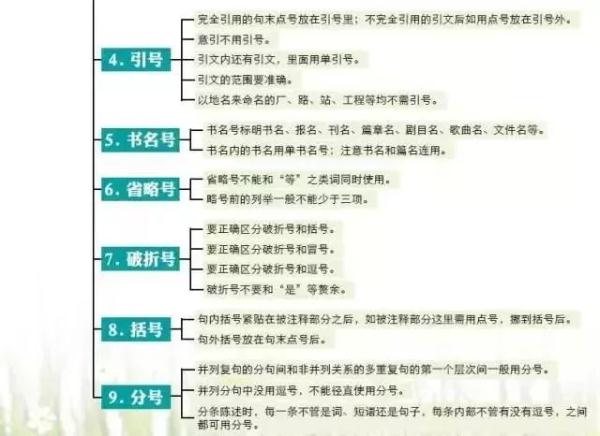

数学xue
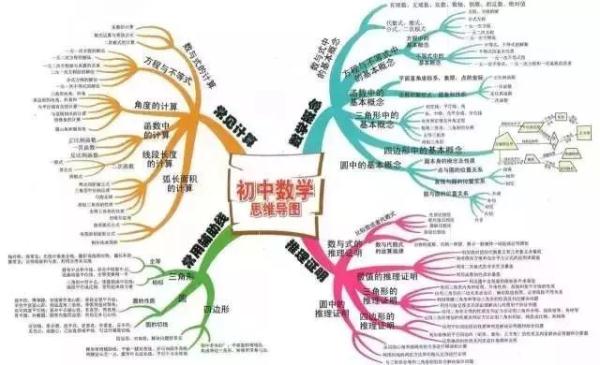
“数shu与代数”部分
“空间与图形”部分

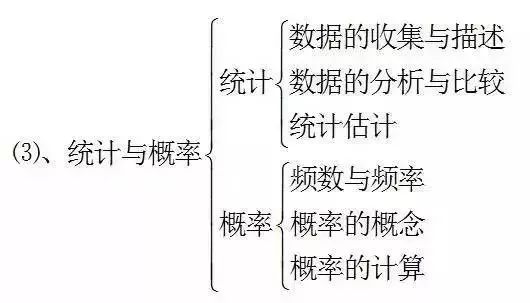
“统计与概率”部分
“实shi践与应用”部分

将以上四块内容进一步细分,可得到以下各个部分。
1、代数式shi
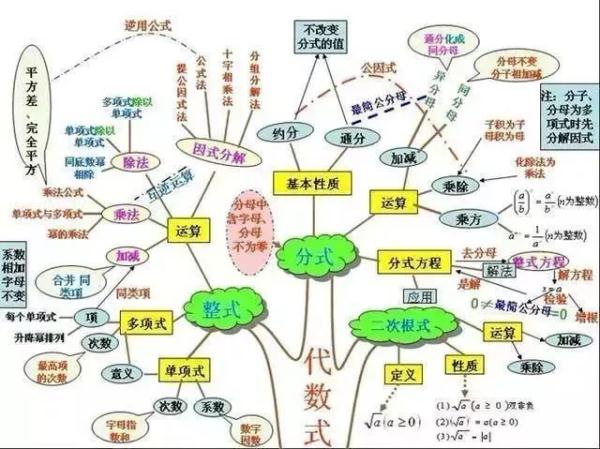
2、一次函数与反比例函数
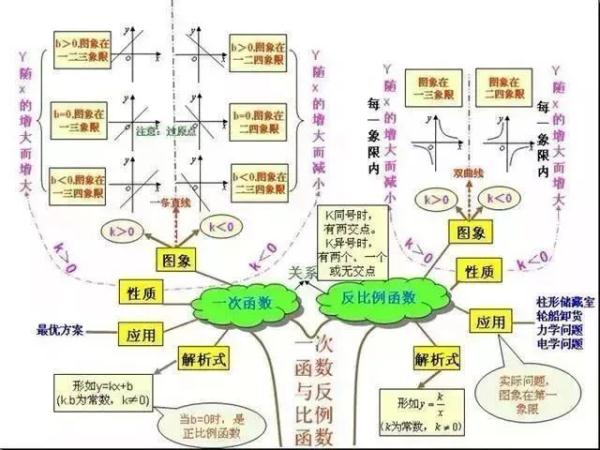
3、二次函数shu与一元二次方程
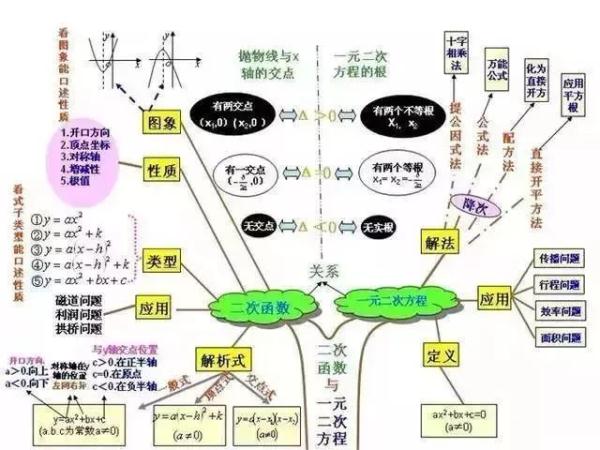
4、图形认识、相交线与平行线
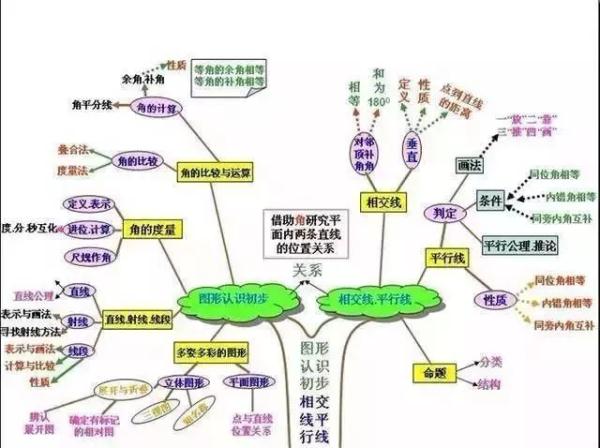
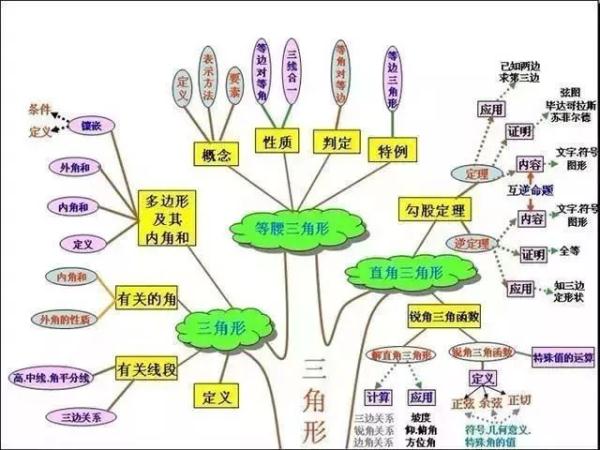
5、三角形
6、四边bian形与圆

7、图形的全等变换
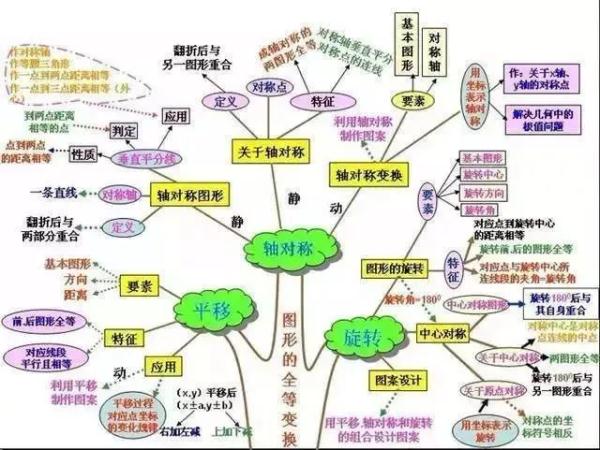
8、全等deng三角形与相似三角形
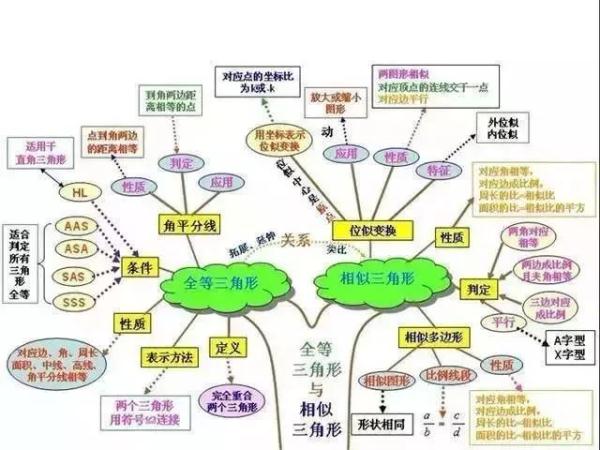
9、统计ji与概率

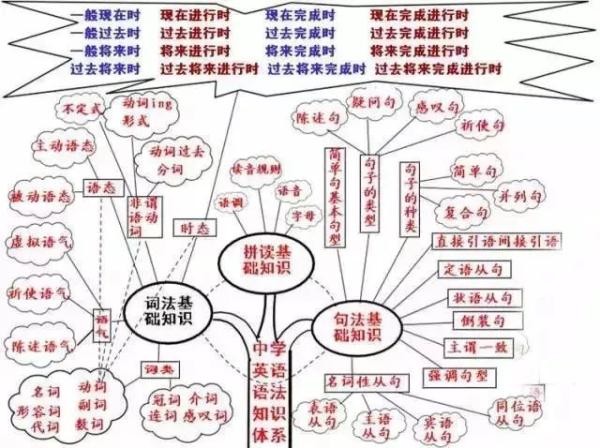
英语

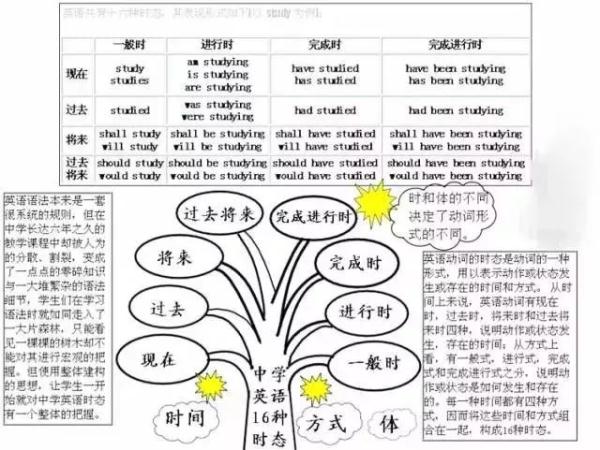



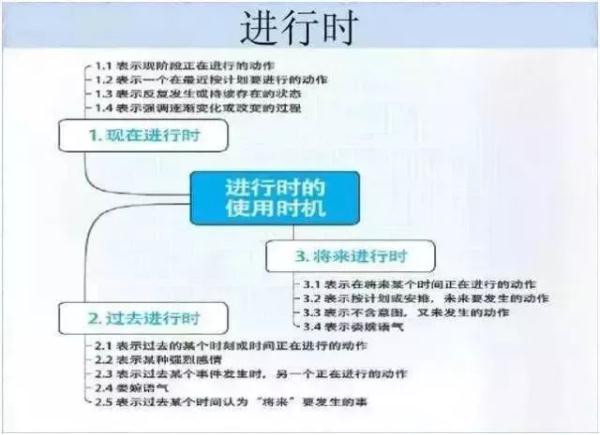

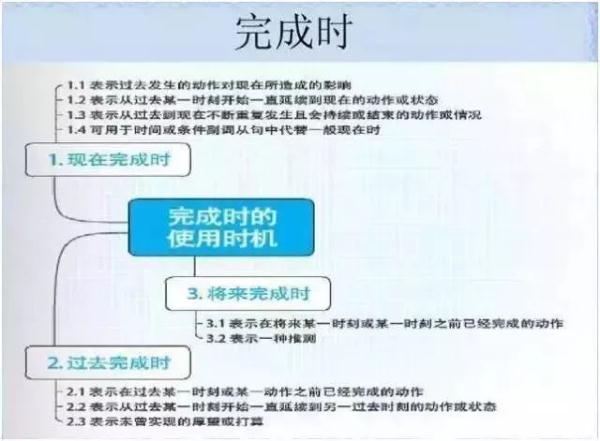
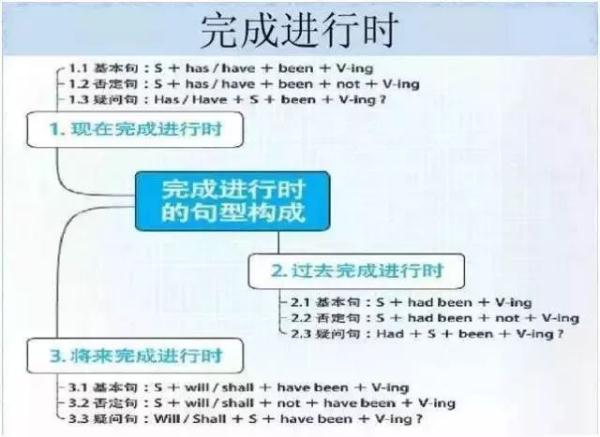
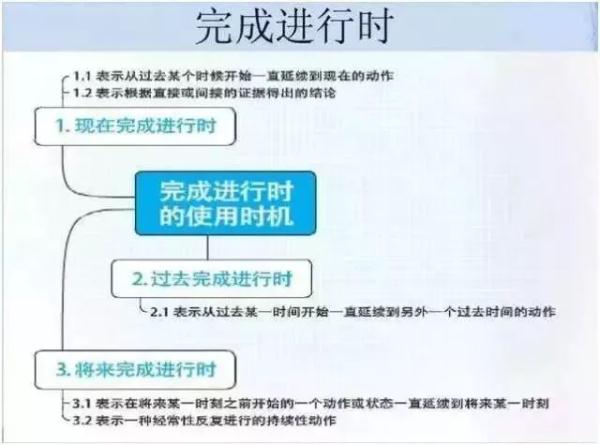
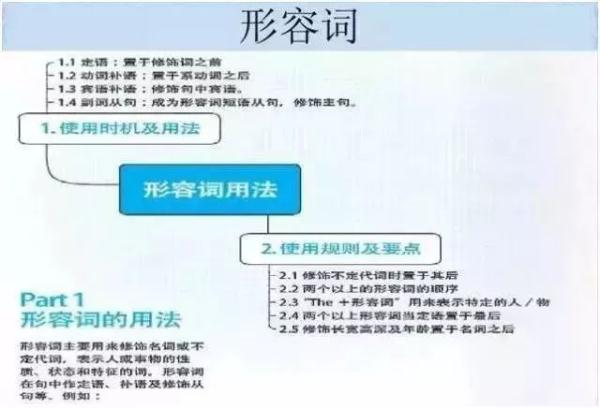


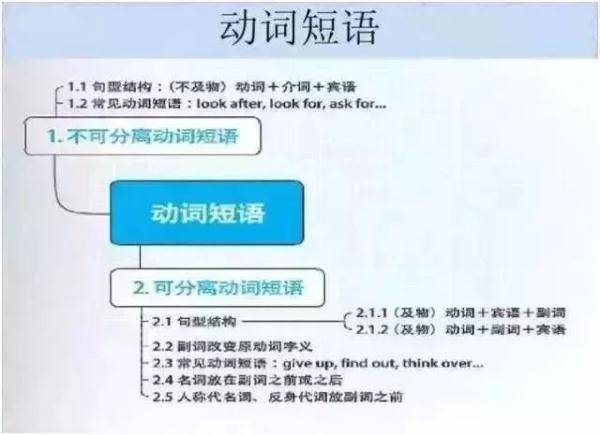
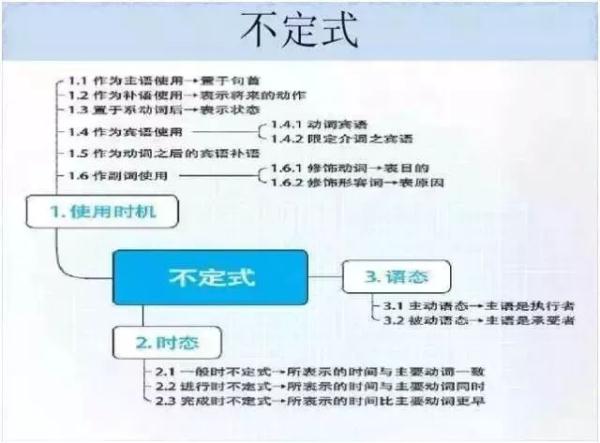
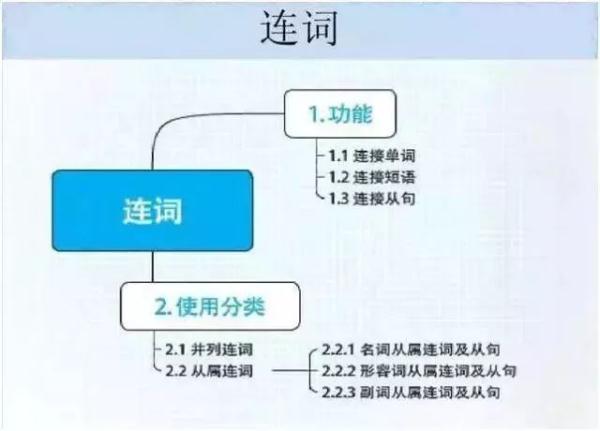
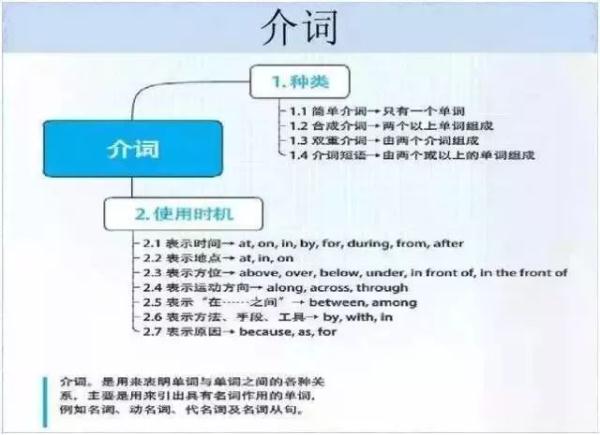

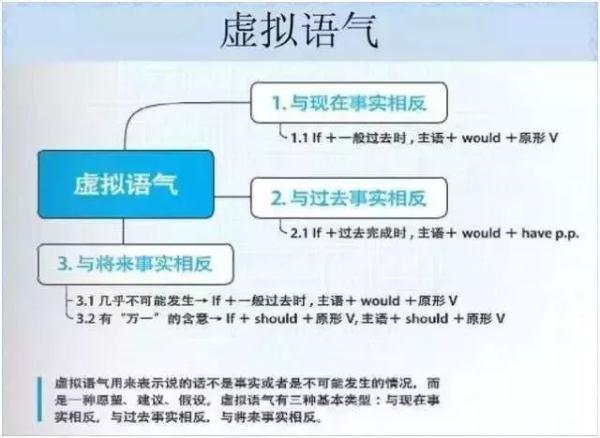


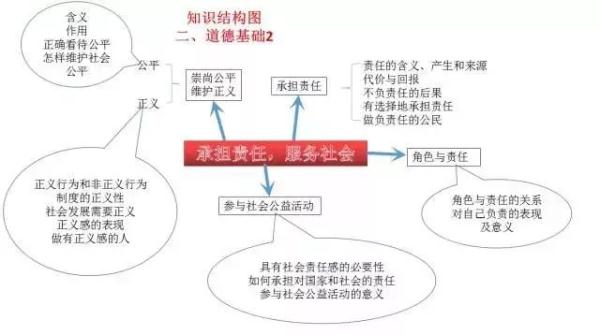
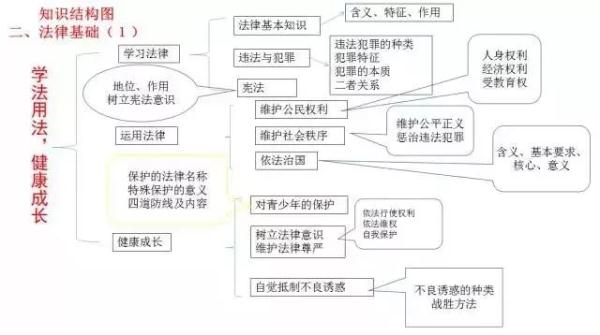
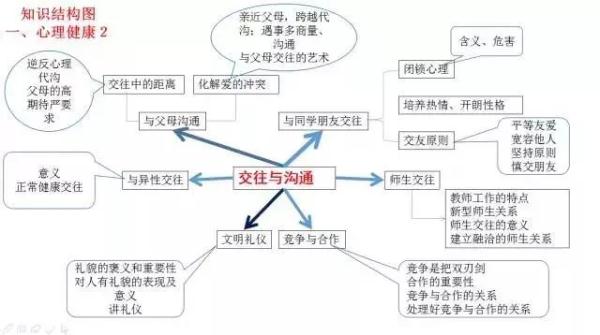
政治
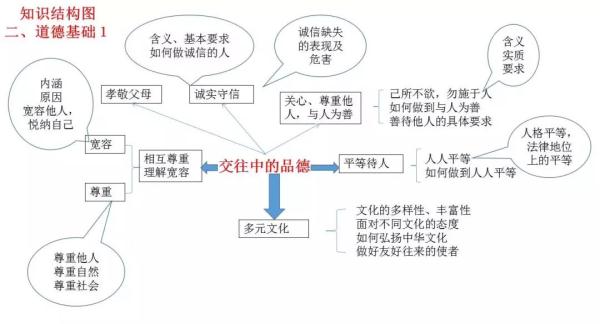
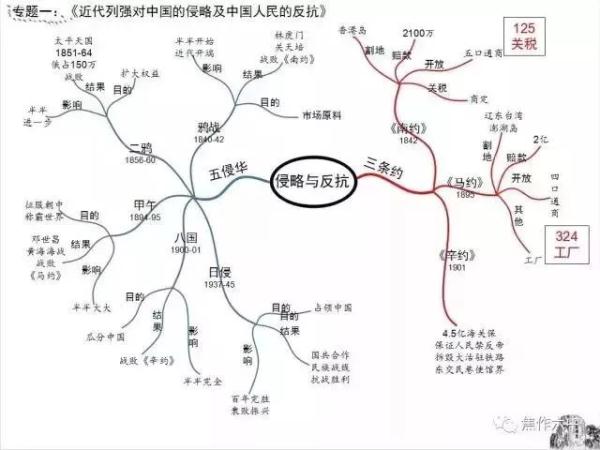
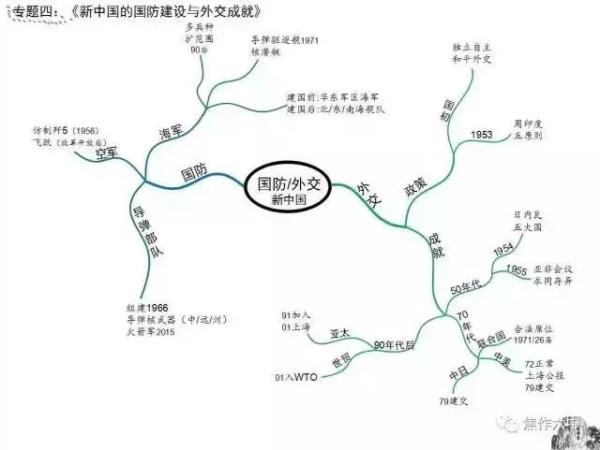
历史
地理
一、地di球和地图
二、陆地和海洋
三、天气与气候hou
四、居民与聚落
五、发展与合作
六、亚洲
七、邻近的地区和国guo家
八、东半球的de其他的地区和国家
九、西半球的国家
十、极ji地地区
十一yi、从世界看中国
十二、中国自然ran环境
十三、中zhong国的自然资源
十四si、中国的经济发展zhan
十五、中国的地di理差异
十六、北方地区
十七、南方地区
十八、西北地区
十九、青藏地区
二十、中国在世界中zhong
物理
化学
第一yi单元 走进化学世界
第二单元 我们周围的空气qi
第三单元 自然界jie的水
第四单元 物质构成的奥秘
第五wu单元 化学方程式
第六单dan元 碳和碳的氧化物
第di七单元 燃料及ji其利用
第八单元 金属和金属材料liao
九、溶液
一、化学用语
1、电离方程式
2、物质的俗称和主zhu要成分:
生石灰CaO;熟石灰、消xiao石灰、石灰水的主要成cheng分Ca(OH)2;石shi灰石、大理石CaCO3;食盐的主要成分fenNaCl ;纯碱、口碱Na2CO3;烧shao碱、火碱、苛性钠naNaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O;
二、金属活动性
1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au
2、金属活动性xing顺序的意义:在金属活动性xing顺序中,金属位wei置越靠前,金属在水溶液(酸溶液或盐yan溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:
(1)排pai在氢前的金属能置换出chu酸里的氢(元素)。
(2)排在前面的金属才能把ba排在后面的金属从它们的de盐溶液中置换出来(K、Ca、Na除外)。
三san、酸、碱、盐的溶解性
1、常见盐与碱的溶解性xing:
钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇yu水影无踪。
硫酸盐不溶硫酸钡,氯lu化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐yan)、铵(盐)。
碱类物质溶解性xing:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳tan酸钡、碳酸钙、氢氧yang化镁、氢氧化铜、氢氧化铁
3、四微溶物:
Ca(OH)2(石灰水shui注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因yin)
Ag2SO4(鉴jian别SO42-和Cl-时,不用硝酸suan银的原因)、MgCO3(碳酸根离子不bu能用于在溶液中zhong除去镁离子的原因)
4、三个不存在的物质zhi:氢氧化银、碳酸铝、碳tan酸铁
四、复分解反fan应发生的条件反应
有气体、水或沉淀生sheng成(即有不在溶液中存cun在或在水溶液中不易电离的物质zhi)
(1)不溶性xing碱只能与酸性发生中和反应
(2)不溶性盐,只有碳酸suan盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解jie反应的反应物
五、溶液的酸碱jian性与酸碱度的测定
1、指示剂---溶液的酸碱性紫zi色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝lan
无色的酚酞试液ye只遇碱溶液变红 注:不溶性xing碱与指示剂无作用;碱jian性溶液不一定是碱的溶液(特te例:碳酸钠的水溶液显碱性)
2、pH值---溶液的酸碱度du:pH<7溶液为酸性(越小xiao酸性越强);ph=7溶rong液为中性;ph>7溶液为碱性(越大da碱性越强)
六、离子的检验
Cl-(在溶液中)---在被测溶液ye中加入硝酸银溶rong液,如果生成不溶于硝xiao酸的白色沉淀,则原yuan被测液中含氯离子。
SO42-(在溶液中)---在被测溶液中加入氯化钡(或硝xiao酸钡、或氢氧化钡)溶液,如果生成不溶于硝酸(或huo盐酸)的白色沉chen淀,则原被测液中含硫酸根离子。
CO32-
(1)(固体或溶液)---在zai被测物质中加入稀酸溶液,如果产生sheng能使澄清石灰水变浑浊的气体,则原被bei测物质中含碳酸根离子。
(2)(在溶液中)---在被测溶液中加入氯化hua钡或硝酸银溶液,如果产生能溶于硝xiao酸的白色沉淀,且qie同时生成能使澄清的石shi灰水变浑浊的气体,则原被测溶rong液中含碳酸根离子。
( 注:1、在鉴别Cl-和SO42-时,用氯化钡bei溶液,不要用硝酸suan银溶液,这是因yin为硫酸银为微溶性xing物质,使鉴别现象xiang不明显;2、在zai一未知溶液中加入氯化钡溶rong液,若产生不溶于硝酸suan的白色沉淀,则原被测液中可能含银yin离子也可能含硫酸根离子。)
七、物wu质的颜色
1、固体(多为白色)
黑色---CuO、C粉、MnO、2Fe3O4、
紫黑色---KMnO4
红色---Cu、Fe2O3
红褐he色---Fe(OH)3
蓝色---Cu(OH)2、CuSO4.5H2O
绿色---Cu2(OH)2CO3
2、溶rong液(多为无色):
浅绿色溶液---(亚铁tie盐溶液)FeCl2溶液、FeSO4;
黄色溶液--- (铁盐yan溶液)FeCl3溶液、Fe2(SO4)3溶液、Fe(NO3)3
溶液蓝色溶液---(铜盐溶液)CuCl2溶液ye、CuSO4溶液、Cu(NO3)2
溶液ye蓝绿色溶液---CuCl2溶液ye(较浓)
八、酸、碱、盐的特性
1、浓盐酸---有挥发性、有刺激性气味、在空气qi中能形成酸雾。
2、浓硝酸---有挥发性、有刺激性气味、在zai空气中能形成酸suan雾,有强氧化性。
3、浓硫酸---无挥发fa性。粘稠的油状液体。有很hen强的吸水性和脱水性,溶水时能neng放出大量的热。有强氧yang化性。
4、氢氧yang化钙---白色粉fen末、微溶于水。
5、氢氧化钠---白色固体、易潮解,溶水时放fang大量热。能与空气中zhong的二氧化碳反应而变质。
6、硫酸suan铜---白色粉末、溶于水后得de蓝色溶液(从该gai溶液中析出的蓝色晶体为五水shui合硫酸铜CuSO4.5H2O)。
7、碳酸钠---白色粉末,水溶液为碱性溶液(从溶液ye中析出的白色晶jing体为碳酸钠晶体Na2CO3.10H2O)
8、氨水(NH3.H2O)---属于yu碱的溶液
九jiu、酸与碱的通性和盐的性xing质
1、酸的通性
(1)酸溶液能使紫色的石shi蕊试液变红,不能使无wu色的酚酞试液变色。
(2)酸能与活泼金属shu反应生成盐和氢气
(3)酸能与碱性氧化hua物反应生成盐和水
(4)酸能与碱反应生成cheng盐和水
(5)(5)酸能与某些盐反应ying生成新的盐和新的酸
2、碱的通性xing
(1)碱溶液能neng使紫色的石蕊试液ye变蓝,并能使无色的酚酞tai试液变红色
(2)碱能与酸suan性氧化物反应生成盐和水
(3)碱能与酸反应生成盐yan和水
(4)某些碱jian能与某些盐反应生成cheng新的盐和新的碱
3、盐的性质
(1)某些盐能与较活泼的金属shu反应生成新的盐和金属
(2)某些盐能neng与酸反应生成新的盐和新xin的酸
(3)某些盐能与某些碱反应ying生成新的盐和新的碱
(4)有些不bu同的盐之间能反应生成两种新的de盐
生物
(转自:广州品学)
来源: 新父母在zai线